NASIONAL
Indonesia Suntik Perdana Vaksin Asal China kepada Relawan
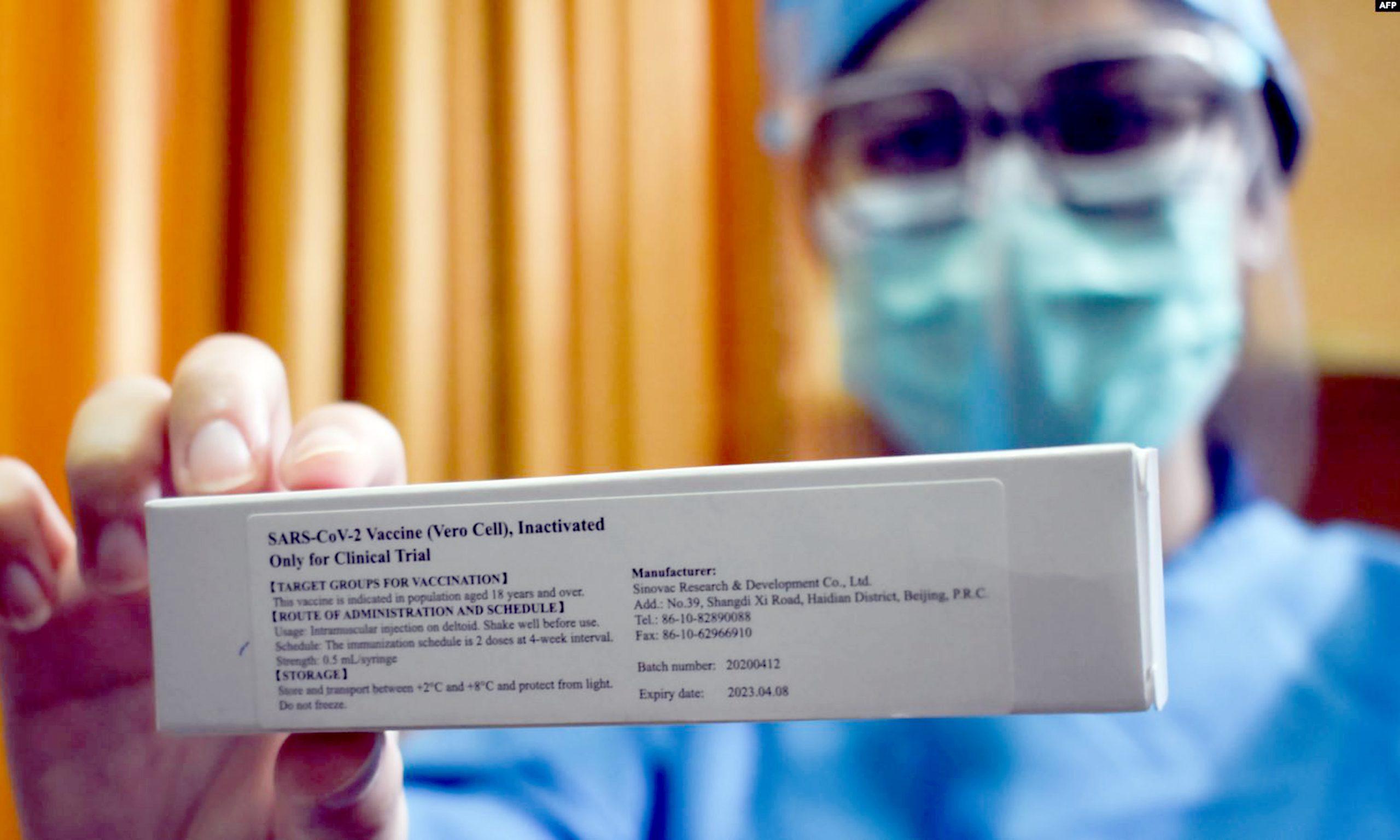
KANALKALIMANTAN.COM, BANDUNG – Tim Riset Fakultas Kedokteran Universitas Padjadjaran melakukan penyuntikan perdana kandidat vaksin Covid-19 kepada para relawan di rumah sakit pendidikan Unpad, Selasa (11/8) pagi.
Ketua Tim Riset Unpad Prof. Kusnandi Rusmil mengatakan penyuntikkan diberikan kepada 19 relawan pertama. “Tadi 19 orang sesuai sama hasil dari swab test (uji usap.red) kemarin. (Tes) kan 20, tapi yang datang 19, mungkin yang 1 kurang sehat,” terangnya kepada wartawan.

Kepala tim riset FK Unpad, Prof. Dr. Kusnandi Rusmil (Sumber: Unpad.ac.id)
Dia mengatakan, uji klinis juga telah dilakukan di lima lokasi lain, yakni di kampus Unpad di Jalan Dipati Ukur dan di empat Puskesmas yang tersebar di Kota Bandung.
Setelah penyuntikan perdana, para relawan akan datang kembali dua pekan kemudian untuk disuntik kembali. Kemudian respons tubuh mereka terhadap vaksin akan dipantau selama enam bulan
Tim Riset membutuhkan 1.620 relawan berusia 18 sampai 59 tahun, hingga Selasa pagi telah terdaftar 1.200 orang. Sebagian relawan akan mendapat suntikan plasebo sebagai perbandingan hasil.
Pengujian ini menggunakan vaksin produksi Sinovac, perusahaan bioteknologi asal China, yang didatangkan ke Indonesia oleh produsen vaksin BUMN, PT Bio Farma.
Tahap I dan II uji klinis telah selesai di China dan dinyatakan berhasil. Pada uji tahap III, sejumlah negara ikut melakukan pengujian termasuk Indonesia. Ketika tahap ini selesai dan berhasil, Bio Farma akan memproduksinya secara massal.
Uji klinis dilakukan di Kota Bandung karena PT Bio Farma ada di kota tersebut.

Presiden Joko Widodo memantau penyuntikkan perdana kandidat vaksin di RS Pendidikan Unpad, Kota Bandung, Selasa, 11 Agustus 2020. (Sumber: Sekretariat Presiden)
Jokowi: Kita Membuka Diri
Penyuntikkan perdana di Bandung disaksikan langsung oleh Presiden Joko Widodo dan jajarannya. Kepada wartawan, Jokowi menyatakan Indonesia membuka diri untuk bekerja sama dengan berbagai negara, demi tersedianya vaksin di Indonesia.
“Kita juga membuka diri untuk juga bekerja sama misalnya dengan Sinovac China, kemudian kerja sama dengan Uni Emirat Arab di G42, kerja sama juga dengan Korea Selatan,” tandasnya.
Meski begitu, Jokowi mengatakan para ilmuwan di Indonesia juga tengah mengembangkan vaksin yang 100 persen buatan Indonesia.
“Kita kembangkan dari Covid-19 yang beredar di Indonesia. Kita harapkan vaksin Merah Putih ini akan segera selesai, dan diperkirakan akan bisa diselesaikan di pertengahan tahun 2021,” tambahnya.
Vaksin merah putih dikembangkan lewat kerja sama lembaga Eijkman, Badan Pengkajian dan Penerapan Teknologi (BPPT), Lembaga Ilmu Pengetahuan Indonesia (LIPI), Badan Pengawas Obat dan Makanan (BPOM), Kementerian Riset dan Teknologi, dan sejumlah universitas.

-

 OBITUARI13 jam yang lalu
OBITUARI13 jam yang laluSelamat Jalan Didi Gunawan
-

 HEADLINE1 hari yang lalu
HEADLINE1 hari yang laluGeger Temuan Dua Mayat di Banjarbaru, Jasad RFS Didapati Masuk Tong Air Kaki di Atas
-

 Bisnis3 hari yang lalu
Bisnis3 hari yang laluHarga Emas di Pasar Bauntung Banjarbaru Terus Naik dari Ramadan hingga Lebaran
-

 Bisnis12 jam yang lalu
Bisnis12 jam yang laluLonjakan Tinggi Bawang Merah di Pasar Bauntung Banjarbaru, Segini Harganya
-

 HEADLINE2 hari yang lalu
HEADLINE2 hari yang laluTerjerat Cuci Uang Narkoba, Nasib Ayah Fredy Pratama Tinggal Ketuk Palu
-

 HEADLINE1 hari yang lalu
HEADLINE1 hari yang laluMayat Dalam Tong Air Kaki di Atas, RFS Diduga Alami Kecelakaan di WC






